Principaux points à retenir :
Ce que les investisseurs devraient surveiller :
- La volatilité de la tarification constitue la nouvelle prime de risque : lorsque les investisseurs ne peuvent plus modéliser avec confiance la tarification et le remboursement aux États‑Unis, les taux d’actualisation augmentent et les programmes marginaux ne sont plus financés. L’incertitude liée aux prix pèse davantage sur une transaction qu’une réduction des revenus.
- La stratégie géographique en dit long sur la confiance dans la tarification : les entreprises qui lancent leur produit aux États-Unis d’abord, tout en retardant le lancement en Europe ou au Canada, protègent l’intégrité de leur tarification par rapport à la référence internationale des prix. Ce changement stratégique dans la séquence de lancement constitue un indicateur précoce de pressions sur les prix.
- La compression de l’écart brut-net révèle le pouvoir de marché : alors que les intermédiaires représentent près de 50 % des dépenses en médicaments aux États-Unis, les fabricants qui maintiennent un écart brut-net inférieur à 40 % font preuve de rigueur en matière de tarification et d’une capacité d’influence sur la liste de médicaments, un indicateur bien plus pertinent que le prix catalogue.
- L’intégration précoce des considérations liées à la tarification sépare les gagnants des perdants : les entreprises qui intègrent la tarification fondée sur la valeur dans la conception des essais de phase 2 (choix des critères d’évaluation, sélection des comparateurs, modélisation médico‑économique) obtiennent de meilleures valorisations que celles qui traitent la tarification comme une étape post‑développement.
- Les flux de capitaux non dilutifs évoluent : les entreprises de biotechnologie en phase initiale ont toujours compté sur des partenariats hors États‑Unis pour valider leurs programmes et prolonger leur horizon financier. Les stratégies privilégiant d’abord le marché américain rendent désormais ces partenariats moins attrayants. Il faut donc s’attendre à une dilution plus importante du capital et à des ententes européennes conclues plus tardivement.
Et la suite ?
- La Chine s’impose comme la variable stratégique : alors que l’incertitude entourant les prix aux États-Unis augmente, l’évolution de la Chine – d’un simple pôle manufacturier à une source d’innovation – crée une pression concurrentielle sur le pouvoir de fixation des prix, les stratégies de propriété intellectuelle et la géographie des essais cliniques.
- Les seuils de valeur augmentent pour tous les payeurs : les médicaments répondant à des besoins médicaux importants (oncologie, maladies rares, thérapies géniques) continueront d’offrir des rendements intéressants, mais seulement si leur valeur ajoutée par rapport aux traitements existants est démontrée. La préparation aux évaluations des technologies de la santé n’est désormais plus facultative.
- Les politiques redéfinissent l’affectation des capitaux et ne se limitent pas aux revenus: depuis l’adoption de l’IRA, plus de 55 programmes de recherche ont été interrompus et 26 médicaments ont été abandonnés. Il faut suivre de près l’exposition par aire thérapeutique à Medicare, à la tarification selon le principe de la nation la plus favorisée et aux calendriers de négociation – désormais des facteurs de risque centraux.
- Le système doit se recalibrer à l’échelle mondiale : pendant des décennies, les États-Unis ont assumé une grande part du risque mondial en recherche et développement grâce à des prix élevés. À mesure que cette dynamique évolue, on peut s’attendre à des hausses de prix internationales, à un accès mondial plus tardif aux médicaments ou à un ralentissement systémique de l’innovation – trois scénarios qu’il faut désormais modéliser.
Introduction
Le débat sur la tarification des médicaments aux États-Unis est souvent présenté comme un argument moral : les Américains ne devraient pas payer plus que les patients d’autres pays pour les mêmes médicaments. Les politiques axées sur le principe de la nation la plus favorisée et la Loi sur la réduction de l’inflation ont été présentées comme des mécanismes permettant de corriger une partie de ce déséquilibre. Mais cette manière de poser le débat passe à côté d’un élément fondamental.
La tarification des médicaments va au-delà de la simple question économique ⎯ et reflète la valeur accordée à l’innovation en santé.
L’année écoulée a été marquée par un revirement rapide du contexte macroéconomique. Les changements apportés aux politiques commerciales ont eu des effets étendus et inégaux dans de nombreux secteurs. Les changements apportés à la FDA, ainsi que la discussion sur les politiques fondées sur le principe de la nation la plus favorisée, ont semé l’incertitude dans le secteur de la biotechnologie. Les fondateurs et les investisseurs veulent comprendre l’incidence des décisions des payeurs sur la valeur de l’innovation.
Pour comprendre la tarification des médicaments, il faut examiner les différents systèmes de remboursement et les principales parties prenantes aux États-Unis par rapport aux marchés qui utilisent l’évaluation des technologies de la santé, comme le Canada, le Royaume-Uni et certains pays européens.
Le paysage de la tarification aux États-Unis et ses acteurs
Pendant des décennies, les États-Unis ont servi de moteur de rentabilité finançant l’innovation pharmaceutique mondiale. Le pays fonctionne selon un système multipayeurs, combinant payeurs privés et publics, l’agence fédérale Centers for Medicare & Medicaid Services (CMS) étant le principal payeur de médicaments. Alors que d’autres pays plafonnent les prix des médicaments, les États-Unis ont recours à un système fondé sur le marché, mais fortement intermédié. Plusieurs étalons de prix et modes de remboursement coexistent, et les coûts pour les patients varient selon la couverture d’assurance et les modalités négociées.
Les acteurs commerciaux se répartissent en plusieurs catégories :
- les fabricants mettent au point les médicaments et fixent le prix catalogue et le coût d’acquisition de gros ;
- les organismes de gestion des soins sont les compagnies d’assurance qui gèrent les régimes de soins de santé ;
- les gestionnaires de régimes d’assurance médicaments sont des intermédiaires de l’industrie. Ils gèrent le volet pharmaceutique du régime pour les organismes de gestion des soins, établissent les listes de médicaments et négocient les remises avec les fabricants ;
- les grossistes gèrent l’entreposage et la distribution des médicaments ;
- les réseaux de prestation intégrés de services sont les réseaux hospitaliers de soins médicaux aux patients. Ils soumettent les demandes de remboursement pour les médicaments administrés dans leurs établissements ;
- les pharmacies dispensent les médicaments (par correspondance, en centre de distribution centralisé, ou à des points de vente de détail).
Tous ces acteurs sont verticalement intégrés, par l’entremise de relations informelles, de fusions, d’acquisitions ou de contrats préférentiels. Les organismes de gestion des soins les plus importants contrôlent maintenant les gestionnaires de régimes d’assurance médicaments affiliés et gèrent la majorité des demandes de remboursement d’ordonnances aux États-Unis.
Près de la moitié du montant brut consacré aux médicaments est captée par les acteurs de la chaîne d’approvisionnement pharmaceutique américaine avant que le produit n’arrive au patient, créant le paradoxe tarifaire.
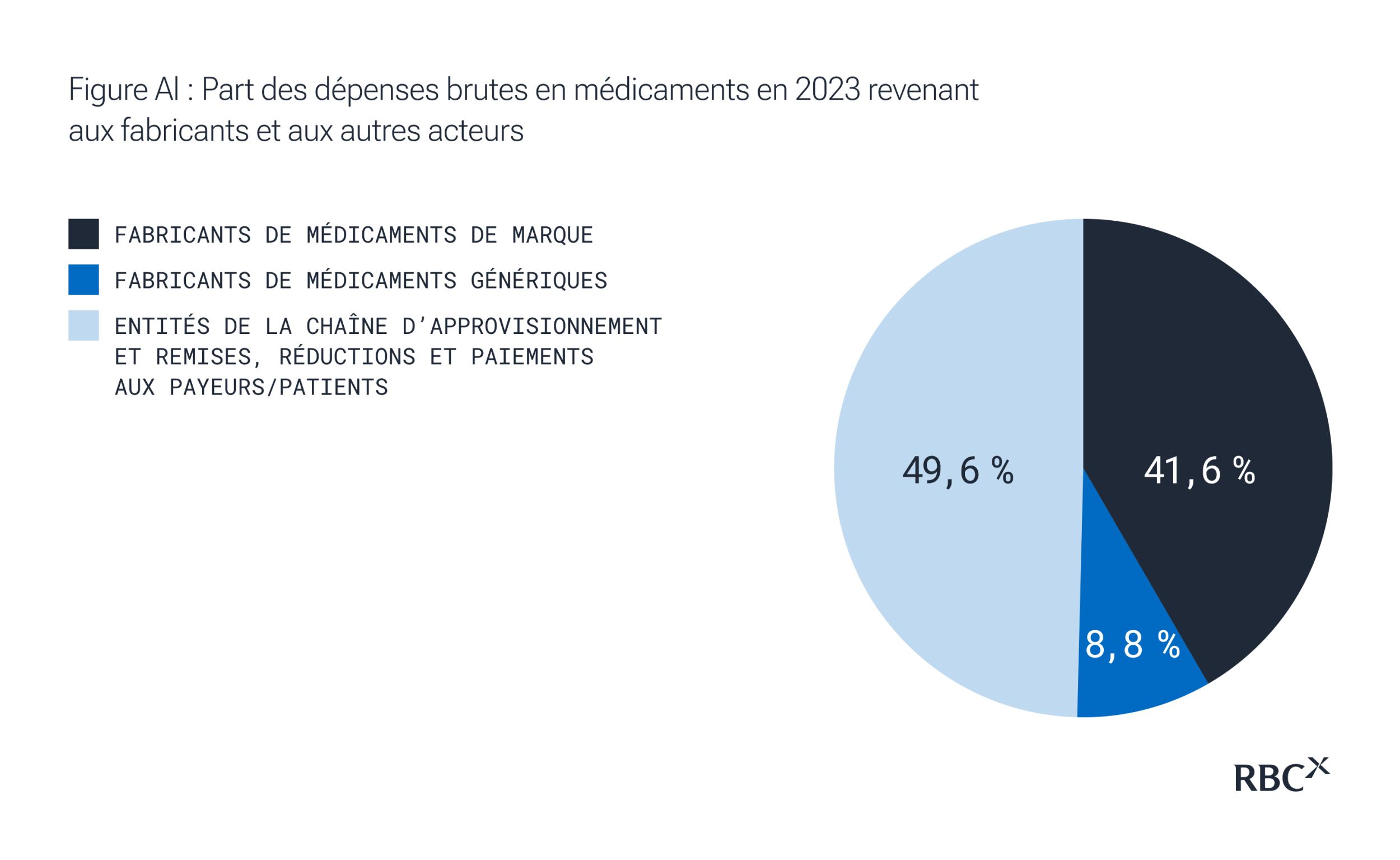
Prix réellement payé par le patient
Avant de lancer le processus de tarification, les fabricants effectuent des recherches sur la volonté de payer auprès des organismede gestion des soins, des gestionnaires de régimes d’assurance médicaments, et des réseaux de prestation intégrés de services, afin d’évaluer le contexte actuel, les comparateurs de prix appropriés et les attentes en matière de contrats et de remises. Les fabricants établissent et publient les prix catalogue, puis négocient un accès privilégié avec les payeurs. Les coûts supportés par les patients découlent d’un enchaînement d’intermédiaires, comme l’illustre la vidéo suivante :
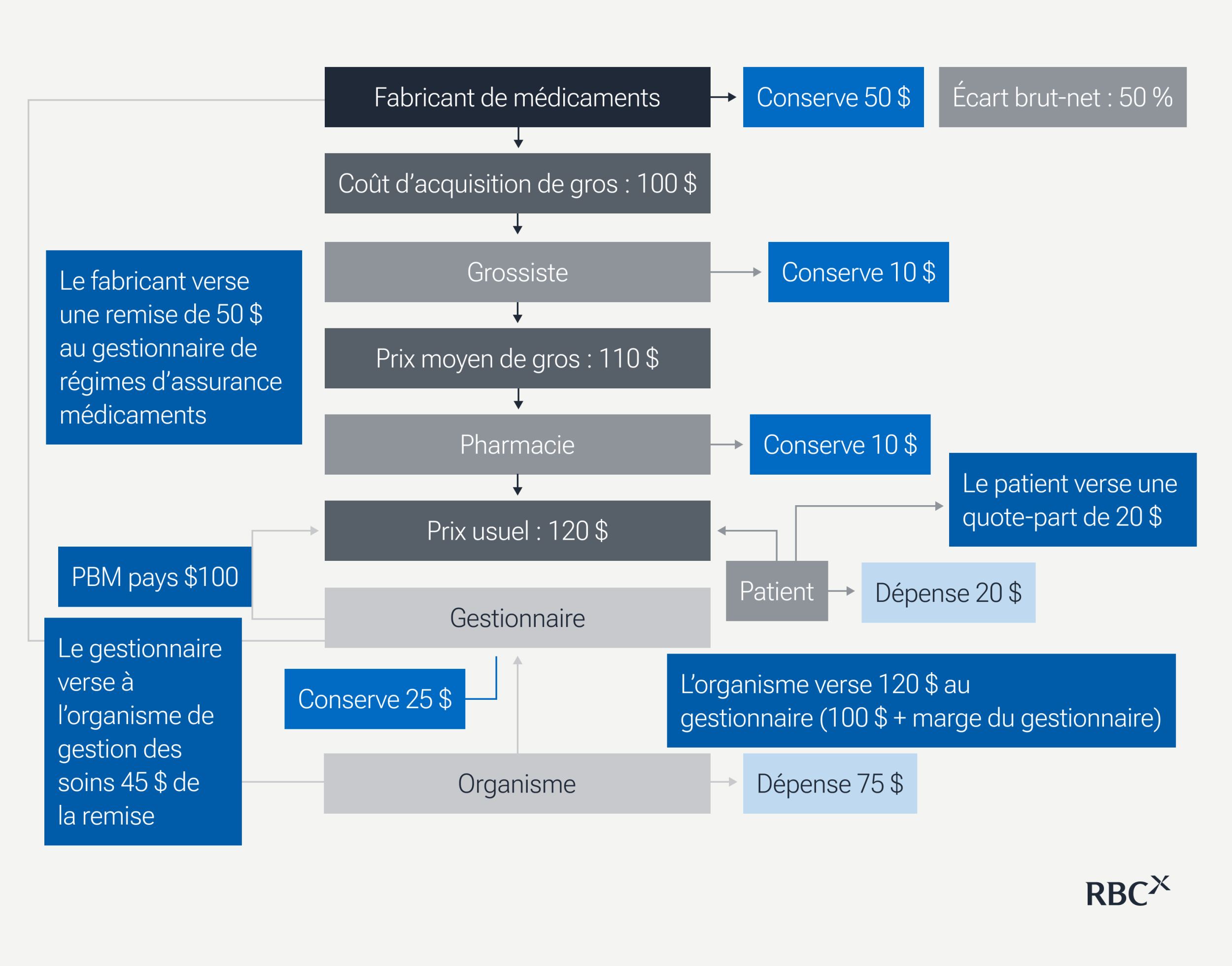
Prenons un médicament hypothétique dont le prix catalogue (coût d’acquisition de gros) est de 100 $. Ce prix catalogue guide l’ensemble du système : les majorations des grossistes, les étalons de remboursement des pharmacies et la négociation de remises.
Déroulement :
- Le fabricant fixe le coût d’acquisition de gros à 100 $, mais verse une remise de 50 $ au gestionnaire de régimes d’assurance médicaments pour figurer sur la liste, ne conservant que 50 $ (réduction de 50 % de l’écart brut-net). Les remises garantissent un statut préférentiel et évitent des restrictions comme les autorisations préalables.
- Le grossiste achète le médicament au coût d’acquisition de gros, gère la distribution et les stocks, et réalise une faible marge (10 $ dans cet exemple). Il assure la disponibilité sans influencer la tarification.
- La pharmacie achète le médicament au prix moyen de gros de 110 $ (prix catalogue de référence), dispense le médicament aux patients, reçoit un remboursement de 100 $ de la part du gestionnaire de régimes d’assurance médicaments, et perçoit une quote-part de 20 $ sur le prix usuel de 120 $, soit le prix de détail standard avant assurance. Les tarifs usuels varient considérablement d’une région à l’autre en fonction des coûts d’exploitation et de la concurrence locale. Cette précision est d’autant plus importante que les patients non assurés paient l’intégralité du prix usuel, et que les assureurs se fient à des étalons de prix usuel par région pour fixer les taux de remboursement et déterminer la quote-part du patient. La marge de 10 $ réalisée par la pharmacie est déterminée par le gestionnaire de régimes d’assurance médicaments.
- Le gestionnaire de régimes d’assurance médicaments agit à titre de gardien financier, contrôlant l’accès aux listes et les négociations avec les fabricants. Il reçoit la remise de 50 $ du fabricant, transfère 45 $ à l’organisme de gestion des soins (il garde 5 $) et conserve la différence de 20 $ entre le prix exigé par l’organisme de gestion des soins (120 $) et le remboursement de la pharmacie (100 $), ce qui représente un total de 25 $.
- L’organisme de gestion des soins verse 120 $ au gestionnaire de régimes d’assurance médicaments, récupère 45 $ en remises, pour un coût net de 75 $. Il compte sur les gestionnaires de régimes d’assurance médicaments pour gérer le volet pharmaceutique du régime tout en maintenant des primes concurrentielles.
- Le patient verse une cote-part de 20 $ calculée sur un prix catalogue gonflé, et non sur le prix net après remise. Il s’agit là d’un enjeu central des politiques publiques. Les patients non assurés (environ 8 % des Américains) paient la totalité du coût usuel, soit 120 $.
Suivre le parcours d’un dollar dans ce système révèle le paradoxe : sur le prix catalogue de 100 $ du fabricant, seulement 50 $ reviennent à l’innovateur qui développe le médicament. Les 50 $ restants sont captés par les intermédiaires : le gestionnaire de régimes d’assurance médicaments conserve 25 $ , le grossiste 10 $, la pharmacie 10 $, et 5 $ représentent les divers écarts. Pour sa part, le patient paie 20 $, une somme calculée sur le prix catalogue gonflé, sans lien avec le coût net réel. Ce système fragmenté absorbe près de 50 % des dépenses en médicaments par l’entremise des intermédiaires, tout en incitant structurellement à des prix catalogue plus élevés pour satisfaire l’ensemble des acteurs. Résultat : les fabricants doivent fixer des prix plus élevés non seulement pour rentabiliser l’innovation, mais aussi pour financer le système de distribution lui-même.
Tarification aux États-Unis comparativement aux marchés qui utilisent l’évaluation des technologies de la santé
Contrairement aux marchés qui utilisent l’évaluation des technologies de la santé, les États-Unis n’imposent aucun plafond au prix de lancement. La tarification reste guidée par le marché, malgré des négociations agressives des payeurs. Les prix nets diminuent avec le temps, mais sans plafonds initiaux imposés par une autorité centrale.
À l’inverse, au Canada :
- Le Conseil d’examen du prix des médicaments brevetés fixe un plafond réglementaire.
- L’Agence canadienne des médicaments (ou l’Institut national d’excellence en santé et en service sociaux [INESSS] au Québec) mène l’évaluation des technologies de la santé pour déterminer la valeur relative par rapport aux traitements existants. Autrement dit, si un fabricant met sur le marché un médicament dans un domaine thérapeutique qui est déjà bien servi par les génériques bon marché, il devra démontrer une amélioration significative par rapport au générique pour faire approuver un prix beaucoup plus élevé.
- Les négociations de remboursement commencent ensuite avec les régimes publics par l’intermédiaire de l’Alliance pancanadienne pharmaceutique ou avec des payeurs privés.
- Même après l’approbation réglementaire, les négociations provinciales, territoriales ou nationales peuvent durer des années.
Le résultat : des prix structurellement plus bas en raison des plafonds réglementaires et de l’accès retardé. Le processus d’approbation de Santé Canada accuse un retard d’environ deux ans par rapport à celui de la FDA. Les investisseurs le savent : les modèles de phase 2 reposent sur les ventes maximales américaines et la durabilité des prix nets aux États‑Unis, pas sur les prix nets allemands ou canadiens.
La vérité qui dérange : la plupart des pays bénéficient depuis des décennies des prix plus élevés aux États‑Unis. Les prix internationaux plus bas persistent parce que les marges américaines absorbent le risque de recherche et développement. Modifier cette dynamique obligerait tout le système mondial à se recalibrer pour trouver un nouveau modèle économique.
Principe de la nation la plus favorisée et IRA : l’enjeu réel dépasse la simple baisse des prix
Actuellement, on suppose que la tarification selon le principe de la nation la plus favorisée ou la négociation relative à l’Inflation Reduction Act (IRA) réduiront radicalement les prix des médicaments aux États-Unis. La réalité est plus nuancée.
En mai 2025, l’administration américaine a signé un décret exécutif exigeant que les Américains ne paient pas plus que le prix le plus bas observé dans les pays de référence (prix selon le principe de la nation la plus favorisée). Cette mesure est distincte de l’Inflation Reduction Act (IRA) de l’ère Biden.
Instaurée en 2022, l’IRA a plafonné à 2 000 $ par année les débours directs des assurés de Medicare pour les médicaments sur ordonnance, transférant la charge des traitements les plus coûteux à Medicare et aux fabricants. Depuis l’adoption de l’IRA, au moins 55 programmes de recherche ont été interrompus et 26 médicaments abandonnés, ce qui soulève des questions quant aux effets des contrôles de prix et des politiques de tarification selon le principe de la nation la plus favorisée sur la découverte de médicaments.
Dans le cadre du programme de négociation des prix des médicaments de Medicare instauré par l’IRA, l’agence CMS fixe les prix équitables maximaux avec les fabricants. La non-conformité de ces seuils entraîne de lourdes pénalités ou la perte d’accès aux marchés Medicare et Medicaid.
L’administration Trump fait également progresser des initiatives de tarification fondée sur le principe de la nation la plus favorisée visant à aligner les coûts des médicaments aux États-Unis sur les références internationales. L’agence CMS a proposé trois nouveaux modèles : Global Benchmark for Efficient Drug Pricing (GLOBE) pour les médicaments relevant de la Partie B, Guarding U.S. Medicare Against Rising Drug Costs (GUARD) pour les médicament relevant de la Partie D, qui lierait les remises des fabricants aux prix internationaux par l’intermédiaire de démonstrations obligatoires de Medicare, et Generating cost Reductions (GENEROUS) pour Medicaid, qui, à ce stade, demeure facultatif. Toujours à l’état de proposition ou de projet pilote, ces modèles visent à utiliser les données de prix internationaux pour réduire principalement les coûts de Medicare et Medicaid. L’impact variera selon le domaine thérapeutique et l’exposition à Medicare.
Même si ces mesures ne sont pas encore finalisées, la perturbation la plus importante n’est pas la perte immédiate de revenus, mais l’incertitude stratégique. Lorsque les investisseurs ne peuvent plus modéliser avec confiance les prix et le remboursement aux États‑Unis, les primes de risque augmentent, les taux d’actualisation montent, les seuils de rendement se déplacent, et les programmes marginaux passent sous la barre de financement.
Une politique de prix n’a pas besoin de réduire les revenus pour influer sur la formation du capital. Il suffit qu’elle augmente la volatilité perçue.
L’innovation n’est pas binaire, elle est marginale
Les décideurs politiques présentent souvent le débat comme une opposition entre accès et innovation, mais la réalité est plus nuancée. Un programme d’oncologie de phase 3 coûtant 2 milliards de dollars est financé lorsque les rendements ajustés au risque dépassent les seuils exigés, et non pour des raisons philosophiques ou altruistes.
Si les prix attendus aux États‑Unis diminuent ou deviennent moins prévisibles :
- Certaines indications ne seront pas poursuivies
- Certains programmes de la phase 2 ne donneront pas droit à une licence
- Certains investissements dans des technologies de plateforme ne seront pas financés
- Certains partenariats précoces ne seront pas conclus
Les entreprises de biotechnologie en démarrage pourraient faire face à de grands défis. Historiquement, le capital non dilutif provenant de partenariats hors États‑Unis permettait à la fois de valider les programmes et de prolonger la marge de manœuvre financière. Si la séquence de lancement évolue vers des stratégies « États-Unis d’abord » – avec un lancement retardé en Europe ou au Canada – ces partenariats deviennent moins attrayants. Les ententes de codéveloppement se transforment en ententes de distribution, les paiements initiaux diminuent, la validation s’affaiblit et la dilution du capital augmente.
La tarification selon le principe de la nation la plus favorisée ne réduira peut-être pas directement l’innovation. Elle pourrait simplement modifier les mécanismes qui la financent.
Changement dans la séquence des lancements
Une conséquence sous-estimée du resserrement de la tarification aux États-Unis est la redéfinition des priorités géographiques. À mesure que les prix aux États-Unis se rapprocheront des références internationales, les entreprises chercheront à préserver l’intégrité de leurs prix en :
- lançant leur produit d’abord aux États‑Unis ;
- retardant les lancements en Europe pour éviter l’ancrage des prix par référencement international ;
- sélectionnant plus soigneusement l’ordre des indications ;
- concevant les essais pour optimiser plus tôt les critères d’évaluation à portée commerciale.
Paradoxalement, les politiques visant à égaliser les prix pourraient accentuer les écarts dans les délais d’accès ou augmenter les coûts dans d’autres marchés.
La valeur continuera de primer — mais il sera plus difficile d’en apporter la preuve
Les médicaments ne représentent qu’une part minoritaire des dépenses de santé dans les pays développés. Les thérapies à forte valeur ajoutée répondant à des besoins médicaux importants (oncologie, maladies rares, thérapies géniques transformantes) continueront d’obtenir des rendements significatifs.
Les payeurs ne sont pas opposés à l’innovation. Ils s’opposent plutôt à l’incertitude et aux dépenses à faible valeur. Mais le seuil d’exigence augmente. La tarification fondée sur la valeur progresse en biotechnologie, et la valeur varie selon les marchés.
Pour les fondateurs, la stratégie de tarification ne peut pas être élaborée après la phase 2. Elle doit orienter :
- la sélection des indications ;
- le choix des comparateurs ;
- la conception des critères d’évaluation ;la modélisation médico‑économique ;
- stratégie d’accès au marché.
L’époque où l’on faisait passer la science avant la tarification est révolue. Les entreprises doivent intégrer la stratégie de prix tôt pour démontrer la valeur et rester compétitives.
Ce que les investisseurs devraient surveiller
Pour les investisseurs, les signaux clés sont les changements structurels, et non les manchettes politiques :
- Les paiements initiaux dans les partenariats diminuent-ils ?
- Les entreprises lèvent-elles plus tôt du capital dilutif ?
- Les domaines thérapeutiques sont-ils plus exposés à Medicare ?
- Les essais de phase 3 sont-ils davantage conçus en fonction des exigences des payeurs ?
- Les lancements à l’extérieur des États-Unis sont-ils systématiquement reportés ?
- Le capital se concentre-t-il dans un plus petit nombre de domaines thérapeutiques jugés plus sûrs ?
Si les réponses penchent vers l’affirmative, cela indique que la réforme des prix influe déjà sur l’allocation du capital — même si les prix affichés semblent stables.
Et la suite ?
Rien de tout cela ne suggère que le système mondial de tarification des médicaments est optimal. Il est coûteux, politiquement sensible et structurellement inefficace. Mais il faut reconnaître un compromis stratégique : la politique de tarification des médicaments ne concerne pas seulement l’accessibilité financière. Elle détermine qui assume le risque biomédical mondial.
Si les États‑Unis réduisent leur volonté de payer pour les nouveaux produits, les autres pays devront décider s’ils sont prêts à assumer une plus grande part de ce « fardeau ». Compte tenu du changement perçu dans la dynamique économique de la tarification des médicaments, on pourrait voir apparaître une augmentation des prix dans les marchés qui utilisent l’évaluation des technologies de la santé.
L’incertitude liée aux prix donne aussi lieu à des occasions. La Chine, autrefois un pôle de fabrication et de génériques, est devenue une source majeure d’innovation. Cette transformation influence le pouvoir de fixation des prix, les stratégies d’essais cliniques, la propriété intellectuelle et la concurrence mondiale. La question n’est pas de savoir si la réforme de la tarification affectera les biotechnologies, mais quelle part du capital consacré à l’innovation le système est prêt à réallouer, voire à déplacer géographiquement.
